電負性(英語:electronegativity,簡寫EN),譯作離子性、負電性及陰電性,是綜合考慮了電離能和電子親合能。
這一概念萊納斯·鮑林於1932年提出。
來説,非金屬元素電負性於2.0,金屬元素電負性於2.0。
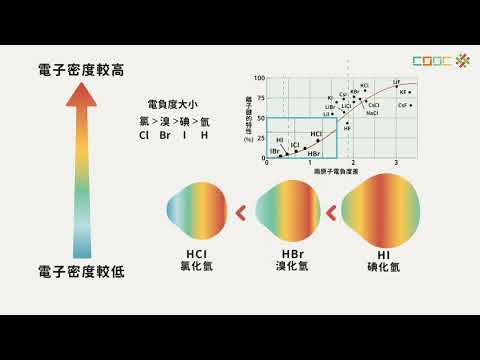

元素電負性數值,原子形成化學鍵時成鍵電子吸引力。
同一週期左右,核電荷遞增,原子半徑遞減,電子吸引能力,因而電負性值遞增;同族元素上到下,原子半徑增大,元素電負性值遞減。
過渡元素電負性值無規律。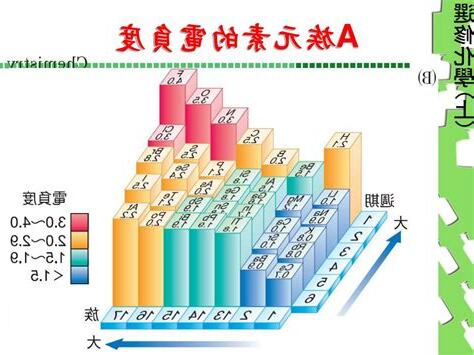
總體而言,週期表右上方典型非金屬元素有電負性數值,氟電負性值數(4.0);週期表左下方金屬元素電負性值,鈁是電負性元素(0.71)。
來説,非金屬元素電負性於2.0,金屬元素電負性於2.0。
電負性概念還可以用來判斷化合物中元素負化合價和化學鍵類型。
電負性值元素形成化合物時,於成鍵電子吸引,往往表現負化合價;而電負性值小者表現化合價。
形成共價鍵時,共用電子會偏移電負性原子而使鍵帶有極性,電負性,鍵極性。
化學鍵兩端元素電負性相差時(例如於1.9)所形成鍵離子鍵主。
元素電負性,吸引電子傾向,非金屬性。
以下所列知識點近10年來化學高考命題中呈現率達90%以上,希望同學們複習中能一一來鞏固相應基礎。


延伸閱讀…
於知識點,以下內容若有誤。
歡迎老師和同學們留言指正。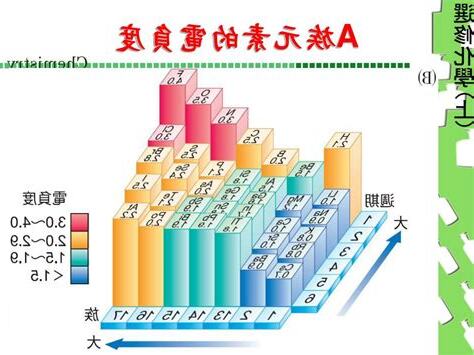
一、俗名無機部分:純鹼、蘇打、天然鹼 、口鹼:Na2CO3小蘇打:NaHCO3大蘇打:Na2S2O3石膏(生石膏):CaSO4.2H2O 熟石膏:2CaSO4·.化學biu一biu,讓你化學biu起來~大家,我是天老師,今天大家講講原電池。
本套講義知識點講解全面,適合查缺補漏和自學,需要必修二全套知識講義可以私信天老師,列印出來,學習效果更佳~今天知識要點有。
以下所列知識點近10年來化學高考命題中呈現率達90%以上,希望同學們複習中能一一來鞏固相應基礎。
延伸閱讀…
10離子反應、離子共存、離子方程式電解質溶液裏起反應,實質上離子之間反應。
離子間反應是趨向於降低離子濃度方向進行。
離子反應離子方程式來表示。
理解掌握離子反應發生條件和正確書寫離子方程式是學離子反應關鍵。
2.(2010•齊齊哈爾高一檢測)氮化矽(Si3N4)是一種新型耐高温耐磨材料,工業上有廣泛的用途,它屬於A.原子晶體 B.分子晶體C.金屬晶體 D.離子晶體【解析】選A。
耐高温、(硬度)是原子晶體性質。
4.序號:6 考點名稱:純鹼工業(侯氏制鹼法) 5年考試次數:3考點內容: 認識考點1、製備原理:侯氏制鹼法是離子反應發生原理進行,離子反應會向著離子濃度減小方向進行(實質勒夏特列原理).
